祝贺课题组博士研究生潘江伟和路兴月的文章被Cell Reports Medicine接收
抗菌药物耐药性已成为全球公共卫生领域面临的重大挑战,铜绿假单胞菌(P. aeruginosa)因其高度的内在耐药性、外膜屏障、生物膜形成能力以及复杂的外排泵系统,被列为临床重点耐药病原体之一,尤其在呼吸系统和创面感染中治疗难度较大。传统单靶点抗生素在临床应用后往往迅速产生耐药突变,提示亟需发展具备多靶点协同机制的新型抗菌策略。金属抗生素(metallo-antibiotics)通过金属离子与抗菌分子的协同作用,能够同时干扰多个细菌生理过程,被认为是克服耐药的重要方向。
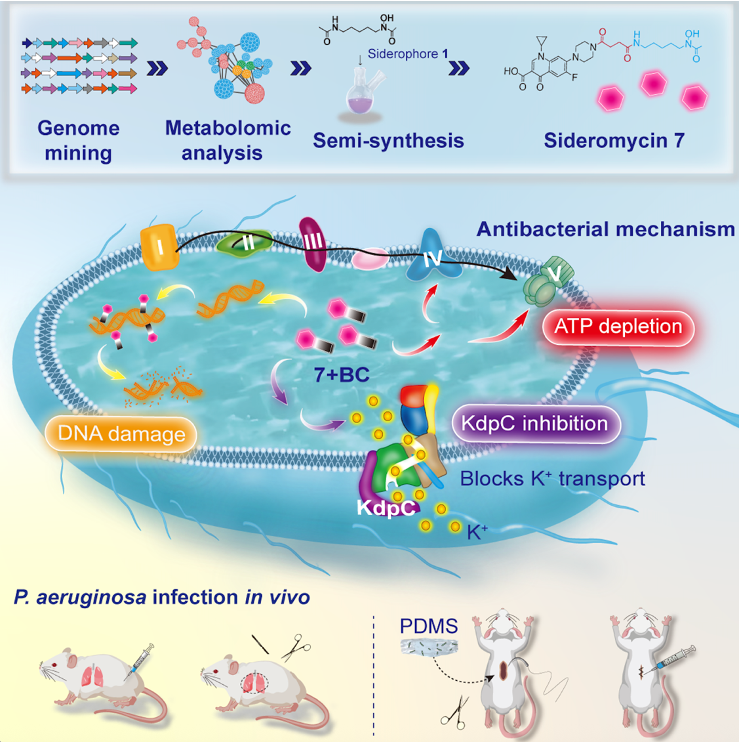
围绕上述研究思路,对3000余株链霉菌的基因组进行去冗余与质量控制,系统解析其次级代谢产物生物合成基因簇(BGCs)的分布特征,并重点挖掘嗜铁素(siderophore)相关基因簇的进化关系与结构多样性。通过antiSMASH 预测、BiG‑SCAPE 网络聚类及序列比对分析,本研究揭示了嗜铁素生物合成基因簇在链霉菌中具有高度保守性,同时仍存在较大的结构创新空间。在此基础上,课题组对筛选获得的目标链霉菌进行次级代谢产物的代谢组学分析与分离纯化,最终得到4个新型嗜铁素类化合物。化学信息学研究显示,新型嗜铁素1与环丙沙星偶联后具有较高的成药潜力。据此,研究选取嗜铁素1及其类似物与环丙沙星进行偶联,共获得5个铁霉素类化合物。其中,铁霉素7与柠檬酸铋联合用药,在体外对耐环丙沙星铜绿假单胞菌表现出最为显著的抗菌活性;连续传代诱导实验中未检测到耐药性产生。小鼠肺炎模型与皮肤感染模型实验进一步证实,该联合用药方案具有优异的体内抗菌效果与良好的安全性。
机制研究表明,该复合体系通过三重作用路径发挥抗菌效应:其一,直接结合细菌DNA并诱导双链断裂;其二,下调KdpC表达,干扰K⁺跨膜转运系统,破坏离子稳态;其三,抑制氧化磷酸化相关蛋白表达,降低ATP生成水平,从能量代谢层面削弱细菌存活能力。多机制协同显著提高了细菌产生耐药的进化门槛。本研究将系统发育基因组学挖掘、铁载体工程设计与金属配位化学策略相结合,提出“多靶点锁定式”抗菌工程理念,为开发新型抗耐药感染药物提供了具有可推广性的技术路径。
该研究以“Phylogenomics-driven metalloantibioticengineering: Overcoming ciprofloxacin resistance in Pseudomonas aeruginosawith sideromycin-bismuth synergy”为题,于2026年2月26日在Cell子刊Cell Reports Medicine上在线发表,浙江工业大学为第一完成单位;药学院/绿色制药协同创新中心陈建伟副教授、博士生潘江伟和路兴月为共同第一作者;海洋药物团队陈建伟副教授与王鸿教授为共同通讯作者。该研究得到国家自然科学基金国际合作与交流项目 NSFC - ASRT(W2412100)以及国家自然科学基金项目(82574317,42276137)的资助。本研究工作合作单位包括:福建省微生物所江红教授团队,浙江大学医学院附属第二医院李江涛教授团队,黑龙江省科学院微生物所于冲副教授团队,浙江省人民医院张大宏教授团队。

